Cuo Tác Dụng Với Dung Dịch H2So4 – Cuo ra CuSO4

Cuo + H2So4 Loãng – Cuo Tác Dụng Với Dung Dịch H2So4 – Cuo ra CuSO4
Phương trình phản ứng giữa đồng (II) oxit và axit sunfuric là một phản ứng hóa học thuộc dạng oxit bazơ tác dụng với dung dịch axit tạo thành muối mới và nước. Đây cũng còn được gọi là một phản ứng trung hòa thường gặp trong chương trình hóa học lớp 8 hoặc lớp 9. Hãy cũng theo dõi nội dung để nắm rõ hơn về phương trình phản ứng và các dạng bài tập hóa học liên quan nhé các em.

cuo h2so4 cuso4 h2o
I – Phương trình phản ứng cuo h2so4 – Cuo ra CuSO4
CuO+H2SO4=CuSO4+H2O đây chính là phương trình hóa học được trổ tài qua công thức hóa học của từng chất. Trong số đó:– CuO là một oxit bazơ.- H2SO4 là một axit mạnh.- CuSO4 là một muối.- H2O là nước.
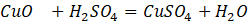
Trong phản ứng hóa học trên, tất cả chúng ta không thấy có sự thay đổi hóa trị hay nói cách khác là không có sự thay đổi số oxi hóa của các chất. Do vậy, phản ứng trên là phản ứng trao đổi bình thường. Cuo + h2so4 không phải là phản ứng oxi hóa – khử như nhiều bạn đang tìm kiếm thông tin trên mạng.Nếu tất cả chúng ta thay đổi điều kiện của phản ứng thì sao?Trong phản ứng hóa học trên, việc thay đổi điều kiện cũng không có quá nhiều. Đơn giản có thể thấy CuO là không thể thay đổi được rồi và tất cả chúng ta chỉ còn có thể thay đổi h2so4 thành axit đặc hoặc các điều kiện khác như h2so4 đặc nguội, h2so4 đặc nóng dư thì cũng đều cho một kết quả giống nhau đó chính là tạo thành muối đồng (II) sunfat và nước. Để lí giải điều này, tất cả chúng ta hãy xem xét vào hóa trị của đồng trong hợp chất cuo.Trong hợp chất cuo, đồng đang có hóa trị là II hay số oxi hóa cao nhất của đồng là +2 rồi nên khi tác dụng với những chất oxi hóa mạnh thì ion đồng cũng không còn khả năng thay đổi hóa trị hoặc số oxi hóa nữa. Do vậy, cuối cùng tất cả chúng ta sẽ thu được một sản phẩm như nhau ở những điều kiện phản ứng khác nhau.Phương trình phản ứng hóa học của CuO với H2SO4 ở nhiều điều kiện khác nhau- CuO+H2SO4=CuSO4+H2OPhản ứng trên xảy ra với điều kiện h2so4 là một axit loãng, như vậy cuo có tác dụng với h2so4 loãng.- CuO+H2SO4 đặc = CuSO4 + H2OPhản ứng trên xảy ra với điều kiện h2so4 là một axit đặc.- CuO+H2SO4 đặc nóng = CuSO4+H2OPhản ứng trên xảy ra với điều kiện h2so4 đậm đặc và được đun nóng. Một thắc mắc cũng được rất nhiều bạn tìm kiếm đó chính là CuO+H2SO4 đặc nóng ra SO2 ?Câu trả lời ở đây làCuO+H2SO4 đặc nóng không thể tạo ra được SO2 các em nhé vì như thầy đã phân tích ở trên. Đây không phải là phản ứng oxi hóa- khử do vậy sẽ không tạo thành SO2 được.- CuO + H2SO4 đặc nguội = CuSO4 + H2O
CuO + H2SO4 đặc nóng có phải phản ứng oxi hóa khử?
Trong nhiều dạng bài tập hóa học tất cả chúng ta đều biết tới CuO là một oxit đồng (II) có được thi thực hiện phản ứng khác là cho Cu tác dụng với Oxi ở nhiệt độ cao. Trong chương trình hóa học lớp 8 tất cả chúng ta vận dụng quy tắc hóa trị sẽ xác nhận được hóa trị của đồng là II bằng với hóa trị của oxi là II và sau này tất cả chúng ta học lên cao sẽ thấy rằng trong hợp chất trên đồng đang có số oxi hóa là +2 cao nhất rồi nên đồng trong hợp chất CuO sẽ không còn số oxi hóa nào để thực hiện phản ứng nữa.Từ những dữ liệu trên tất cả chúng ta tổng kết được ngay phản ứng trên khi thực hiện sẽ không phải là phản ứng oxi hóa – khử.Vậy những hợp chất nào của đồng có thể thực hiện được với H2SO4 đặc nóng phản ứng oxi hóa – khử ?Trong một phản ứng oxi hóa khử điều nhận thấy trước tiên nhất chính là có sự thay đổi số oxi hóa của đơn chất hoặc các chất trong hợp chất nên những hợp chất nào của đồng mà đồng có số oxi hóa khác +2 thì khi tác dụng được với H2SO4 đặc nóng khả năng cao là một phản ứng oxi hóa khử.Ví dụ:Cu + H2SO4 đặc nóng→CuSO4 + SO2 + H2OCu2O + H2SO4 đặc nóng→CuSO4 + SO2 + H2O
II – Các dạng bài tập hóa học liên quan.
Từ phương trình phản ứng hóa học trên tất cả chúng ta thấy rất nhiều dạng bài tập liên quan và được mở rộng vô cùng phong phú. Một trong những dạng bài tập hóa học nền tảng đó chính là tính theo phương trình hóa học.Ví dụ 1: Cho 8 gam CuO tác dụng hoàn toàn với dung dịch axit sunfuric vừa đủ. Sau phản ứng thu được m gam muối.- Viết phương trình phản ứng hóa học.- Tính m = ?Bài giải:- Số mol của CuO là 0,1 mol.- CuO + H2SO4 = CuSO4 + H2O 0,1 0,1Vậy khối lượng muối tạo thành sau phản ứng là 0,1 . (64 + 32 + 64) = 16 gam.Như vậy, ở những phương trình phản ứng và một vài ví dụ bài tập trên các em đã nắm được những thông tin rất thiết yếu về một phương trình phản ứng hóa học vô cơ rồi. Tuy nhiên, trên thực tiễn còn có nhiều điều kiện khác nhau nữa để phương trình có thể xảy ra do vậy thầy rất cần sự đóng phản hồi kiến từ các em qua comment ở bên dưới để nội dung thêm phong phú và hoàn thiện hơn. Xin cảm ơn quý độc giả, các em học sinh đã gắn bó xây dựng ngân hàng phương trình phản ứng hóa học.
Nội dung còn tiếp tục update
Tác giả nội dung: Thầy Liêm
Đề tài: H2O, H2SO4, CuO, CuSO4
Sài Gòn Metro Mall Chúc các bạn học tập tốt

