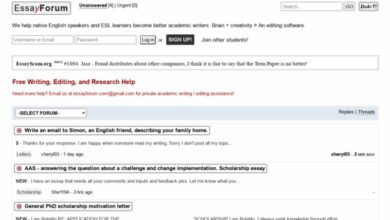
Cu + HNO3 = Cu(NO3)2 + H2O + NO2
Điều kiện phản ứng
Không có
Cách thực hiện phản ứng
cho đồng tác dụng với dd axit HNO3
Hiện tượng nhận thấy
Chất rắn màu đỏ của Đồng (Cu) tan dần trong dung dịch và sủi bọt khí do khí màu nâu đỏ Nito dixoit (NO2) sinh ra.
Thông tin thêm
Axit nitric HNO3 oxi hoá được hầu hết các kim loại, kể cả kim loại có tính khử yếu như Cu. Khi đó, kim loại bị oxi hoá đến mức oxi hoá cao và tạo ra muối nitrat. Thông thường, nếu dùng dung dịch HNO3 đặc thì sản phẩm là NO2, còn dung dịch loãng thì tạo thành NO.
Advertisement
Phương Trình Điều Chế Từ Cu Ra Cu(NO3)2
Trong thực tiễn, sẽ có thể nhiều hơn 1 phương pháp điều chế từ
Cu (đồng) ra
Cu(NO3)2 (Đồng nitrat)
Xem toàn bộ phương trình điều chế từ Cu (đồng) ra Cu(NO3)2 (Đồng nitrat)
Phương Trình Điều Chế Từ Cu Ra H2O
Trong thực tiễn, sẽ có thể nhiều hơn 1 phương pháp điều chế từ
Cu (đồng) ra
H2O (nước)
Xem toàn bộ phương trình điều chế từ Cu (đồng) ra H2O (nước)
Phương Trình Điều Chế Từ Cu Ra NO2
Trong thực tiễn, sẽ có thể nhiều hơn 1 phương pháp điều chế từ
Cu (đồng) ra
NO2 (nitơ dioxit)
Xem toàn bộ phương trình điều chế từ Cu (đồng) ra NO2 (nitơ dioxit)
Phương Trình Điều Chế Từ HNO3 Ra Cu(NO3)2
Trong thực tiễn, sẽ có thể nhiều hơn 1 phương pháp điều chế từ
HNO3 (axit nitric) ra
Cu(NO3)2 (Đồng nitrat)
Xem toàn bộ phương trình điều chế từ HNO3 (axit nitric) ra Cu(NO3)2 (Đồng nitrat)
Phương Trình Điều Chế Từ HNO3 Ra H2O
Trong thực tiễn, sẽ có thể nhiều hơn 1 phương pháp điều chế từ
HNO3 (axit nitric) ra
H2O (nước)
Xem toàn bộ phương trình điều chế từ HNO3 (axit nitric) ra H2O (nước)
Phương Trình Điều Chế Từ HNO3 Ra NO2
Trong thực tiễn, sẽ có thể nhiều hơn 1 phương pháp điều chế từ
HNO3 (axit nitric) ra
NO2 (nitơ dioxit)
Xem toàn bộ phương trình điều chế từ HNO3 (axit nitric) ra NO2 (nitơ dioxit)
Phản ứng oxi-hoá khử
Phản ứng oxi hóa khử thường liên quan đến việc chuyển nhượng điện tử (electron) giữa các đối tượng hóa học.
Để hiểu được trọn vẹn phản ứng oxi hoá khử bạn cần hiểu
Chất khử: chất khử là chất cho electron, nói cách khác, chất khử sẽ có số oxi hoá tăng sau thời điểm phản ứng xảy ra. Trong khái niệm của chương trình phổ thông, chất khử cũng được gọi là chất bị oxi hoá.
Chất oxi hoá: trái lại với chất khử, là chất nhận electron. Chất oxi hoá có số oxi hoá tăng sau phản ứng. Chất oxi hoá, trong khái niệm của chương trình phổ thông còn được gọi là chất bị khừ.
Xem toàn bộ Phản ứng oxi-hoá khử
Thắc mắc minh họa
Click để xem toàn bộ thắc mắc có liên quan tới phương trình Cu
+
4HNO3 => Cu(NO3)2
+
2H2O
+
2NO2
Câu 1. Phản ứng hóa học
Cho các phản ứng sau:
MnO2 + HCl (đặc) (t0) → Khí X + … (1);
Na2SO3 + H2SO4 (đặc) (t0)→ Khí Y + … (2);
NH4Cl + NaOH (t0) → Khí Z + … (3);
NaCl (r) + H2SO4 (đặc) (t0) → Khí G + … (4);
Cu + HNO3 (đặc) (t0) → Khí E + … (5);
FeS + HCl (t0) → Khí F + … (6);
Những khí tác dụng được với NaOH (trong dung dịch) ở điều kiện thường là:
A. X, Y, Z, G.
B. X, Y, G.
C. X, Y, G, E, F.
D. X, Y, Z, G, E, F.
Xem lời giải câu 1
A. X, Y, Z, G.B. X, Y, G.C. X, Y, G, E, F.D. X, Y, Z, G, E, F.
Câu 2. Đồng
Cho các dung dịch loãng: (1) AgNO3, (2) FeCl2, (3) HNO3, (4) FeCl3, (5) hỗn hợp gồm NaNO3 và HCl. Số dung dịch phản ứng được với Cu là.
A. 2
B. 5
C. 3
D. 4
Xem lời giải câu 2
A. 2B. 5C. 3D. 4
Câu 3. Số phản ứng xảy ra ở điều kiện thường
Cho các phản ứng sau:
(1) Cu + H2SO4 đặc, nguội (5) Cu + HNO3 đặc, nguội
(2) Cu(OH)2 + glucozơ (6) axit axetic + NaOH
(3) Gly-Gly-Gly + Cu(OH)2/NaOH (7) AgNO3 + FeCl3
(4) Cu(NO3)2 + FeCl2 + HCl (8) Al + Cr2(SO4)3
Số phản ứng xảy ra ở điều kiện thường ?
A. 5
B. 7
C. 8
D. 6
Xem lời giải câu 3
A. 5B. 7C. 8D. 6
Câu 4. Bài toán thể tích
Hòa tan hoàn toàn 1,28 gam Cu vào dung dịch chứa 7,56 gam HNO3 thu được dung dịch X và V lít hỗn hợp khí gồm NO và NO2 (đktc). Cho X tác dụng hoàn toàn với 105 ml dung dịch KOH 1M, sau đó lọc bỏ kết tủa được dung dịch Y. Cô cạn Y được chất rắn Z. Nung Z đến khối lượng không đổi, thu được 8,78 gam chất rắn. Giá trị V là
A. 0,336
B. 0,448.
C. 0,560.
D. 0,672.
Xem lời giải câu 4
A. 0,336B. 0,448.C. 0,560.D. 0,672.
Câu 5. Phản ứng hóa học
Phản ứng nào sau đây là sai ?
A. Cu + 4HNO3 đặc nguội → Cu(NO3)2 + 2NO2 + 2H2O.
B. 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3.
C. 3Zn + 2CrCl3 → 2Cr + 3ZnCl2.
D. CuO + 2HCl → CuCl2 + H2O.
Xem lời giải câu 5
A. Cu + 4HNO3 đặc nguội → Cu(NO3)2 + 2NO2 + 2H2O.B. 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3.C. 3Zn + 2CrCl3 → 2Cr + 3ZnCl2.D. CuO + 2HCl → CuCl2 + H2O.
Câu 6. Kim loại thụ động
Dãy gồm các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3 đặc, nguội là:
A. Cu, Pb, Ag.
B. Cu, Fe, Al.
C. Fe, Al, Cr.
D. Fe, Mg, Al.
Xem lời giải câu 6
A. Cu, Pb, Ag.B. Cu, Fe, Al.C. Fe, Al, Cr.D. Fe, Mg, Al.
Câu 7. Phản ứng hóa học
Cho các phản ứng sau:
(1) Cu + H2SO4 đặc, nguội
(2) Cu(OH)2 + glucozơ
(3) Gly-Gly-Gly + Cu(OH)2/NaOH
(4) Cu(NO3)2 + FeCl2 + HCl
(5) Cu + HNO3 đặc, nguội
(6) axit axetic + NaOH
(7) AgNO3 + FeCl3
(8) Al + Cr2(SO4)3
Số phản ứng xảy ra ở điều kiện thường ?
A. 5
B. 7
C. 8
D. 6
Xem lời giải câu 7
A. 5B. 7C. 8D. 6
Câu 8. Phản ứng hóa học
Cho các phản ứng sau:
(1) Cu + H2SO4 đặc, nguội ; (5) Cu + HNO3 đặc, nguội
(2) Cu(OH)2 + glucozơ ; (6) axit axetic + NaOH
(3) Gly-Gly-Gly + Cu(OH)2/NaOH ; (7) AgNO3 + FeCl3
(4) Cu(NO3)2 + FeCl2 + HCl ; (8) Al + Cr2(SO4)3
Số phản ứng xảy ra ở điều kiện thường ?
A. 5
B. 7
C. 8
D. 6
Xem lời giải câu 8
A. 5B. 7C. 8D. 6
Câu 9. Tìm phát biểu đúng
Cho các phát biểu sau:
(a) Thép là hợp kim của sắt chứa từ 2-5% khối lượng cacbon.
(b) Bột nhôm trộn với bột sắt(III) oxit dùng để hàn đường ray bằng phản ứng nhiệt nhôm.
(c) Dùng Na2CO3 để làm mất tính cứng tạm thời và tính cứng vĩnh cửu của nước.
(d) Dùng bột lưu huỳnh để xử lí thủy ngân rơi vãi khi nhiệt kế bị vỡ.
(e) Khi làm thực nghiệm kim loại đồng tác dụng với dung dịch HNO3, người ta nút ống nghiệm bằng bông tẩm dung dịch kiềm.
Số phát biểu đúng là :
A. 2
B. 3
C. 4
D. 5
Xem lời giải câu 9
A. 2B. 3C. 4D. 5
Câu 10. Bài tập về tính Hóa chất của kim loại
Cho hỗn hợp X gồm Al, Fe, Cu. Dung dịch nào sau đây khi lấy dư không thể hòa tan hết X?
A. HNO3 loãng
B. NaNO3 trong HCl
C. H2SO4 đặc nóng
D. H2SO4 loãng
Xem lời giải câu 10
A. HNO3 loãngB. NaNO3 trong HClC. H2SO4 đặc nóngD. H2SO4 loãng
Câu 11. Thắc mắc lý thuyết về hệ số cân đối của phản ứng Cu + HNO3
Tổng hệ số (các số nguyên, tối giản) của toàn bộ các chất trong phương trình phản ứng giữa Cu với dung dịch HNO3 đặc, nóng là
A. 8
B. 10
C. 11
D. 9
Xem lời giải câu 11
A. 8B. 10C. 11D. 9
Câu 12. Bài tập về tính Hóa chất của đồng và hợp chất
Phương trình hóa học nào sau đây viết sai?
A. Cu + 2FeCl3 –> CuCl2 + 2FeCl2.
B. Cu + 2AgNO3 –> Cu(NO3)2 + 2Ag
C. Fe + CuCl2 –> FeCl2 + Cu.
D. Cu + 2HNO3 –> Cu(NO3)2 + H2.
Xem lời giải câu 12
A. Cu + 2FeCl3 –> CuCl2 + 2FeCl2.B. Cu + 2AgNO3 –> Cu(NO3)2 + 2AgC. Fe + CuCl2 –> FeCl2 + Cu.D. Cu + 2HNO3 –> Cu(NO3)2 + H2.
Câu 13. Thắc mắc lý thuyết về tính Hóa chất của đồng
Kim loại Cu không tan trong dung dịch:
A. HNO3 loãng
B. HNO3 đặc nóng
C. H2SO4 đặc nóng
D. H2SO4 loãng
Xem lời giải câu 13
A. HNO3 loãngB. HNO3 đặc nóngC. H2SO4 đặc nóngD. H2SO4 loãng
Câu 14. Bài toán hỗn hợp kim loại tác dụng với dung dịch HNO3
Hòa tan hoàn toàn hỗn hợp Mg, Al, Fe và Cu trong dung dịch HNO3 (loãng dư) thu được dung dịch X. Cho dung dịch NaOH dư vào dung dịch X được kết tủa Y. Nung kết tủa Y đến khi phản ứng nhiệt phân kết thúc thu được tối đa bao nhiêu oxit
A. 3
B. 2
C. 1
D. 4
Xem lời giải câu 14
A. 3B. 2C. 1D. 4
Câu 15. Xác nhận kim loại
Hòa tan hoàn toàn 5,6 gam kim loại M trong dung dịch HNO3 đặc ,nóng dư thu được 3,92 lít khí NO2 (đktc) là sản phẩm khử duy nhất . Vậy M là
A. Cu
B. Pb
C. Fe
D. Mg
Xem lời giải câu 15
A. CuB. PbC. FeD. Mg